Un CEntre de reference
tourne vers l'AVENIR
La
RECHERCHE
SUR LES MALADIES AUTO-IMMUNES
La recherche fondamentale, translationnelle et clinique est au coeur des activités du CNR auto-immunité de Strasbourg, en partenariat avec les unités INSERM UMRS-1109 (Pr Bahram) et les Hôpitaux Universitaires de Strasbourg

La recherche au CRMR RESO des maladies auto-immunes de Strasbourg
La section de recherche clinique du service de rhumatologie compte actuellement plus de 40 études. La moitié de ces études ont des patients en cours de suivi. L’autre moitié de ces études n’ont soit pas encore commencé à inclure des patients, soit achevées toutes les visites de suivi.
Cette année, nous avons 32 études en phase de recrutement (y compris des études pas encore inclus de patients). Parmi ces études, 19 sont promues par des partenaires académiques et 13 par des partenaires industriels. Ces études couvrent la plupart des maladies rares ou non rares du service. Le nombre d’études varie chaque année.
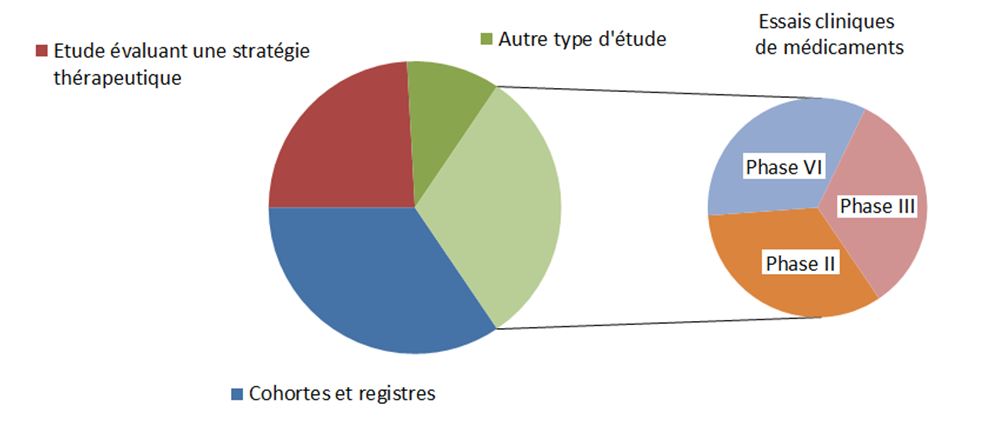
Nous avons maintenant au total 326 patients suivis dans 20 études au sein de service de rhumatologie. Nous avons de nombreux patients atteints d’une maladie auto-immune systémique rare suivis dans des cohortes. Cette approche nous a permis non seulement d’améliorer les connaissances sur la maladie, mais également de mieux suivre les patients en soins de longue durée (Ex: Cohorte européenne de sclérodermie systémique EUSTAR et cohorte nationale de syndrome de Sjörgen primitif ASSESS). De plus, nous sommes en mesure de réaliser les essais complexes de médicaments de phase II ou III qui contribuent au développement de nouveaux médicaments pour traiter les maladies auto-immunes systémiques rares.
Nous proposons une échelle complète de type d’étude (phases II-IV), à l’exception de la phase I de l’essai clinique de médicament, qui doit obligatoirement être réalisée au Centre d’Investigation Clinique (CIC) des Hôpitaux Universitaires de Strasbourg (HUS).
Le nombre de patients inclus dans chaque étude varie considérablement en fonction du type d’étude et de la rareté de la maaldie. Nous avons entre 1 à 7 patients inclus dans les phase II-III des essais cliniques du médicament. Le nombre patients peut atteindre 113 dans une cohorte.
Découvrez nos FAQ sur la recherche clinique
Avant de participer à un essai, le médecin investigateur vous donnera des informations sur l’étude envisagée. Cela vous permettra d’apprendre tout ce qui est attendu de votre part durant le déroulement de l’étude, y compris les contraintes et avantages éventuels, avant de prendre la décision de participer ou non. Vous avez au moins 7 jours pour réfléchir. Le « consentement » désigne un document qui permet de donner, de façon éclairée, libre et par écrit, votre accord de participation à un essai clinique (ou bien celui des titulaires de l’autorité parentale si le participant envisagé est un mineur).
Le consentement a pour but de protéger les participants à une étude clinique en leur fournissant toutes les informations susceptibles de les aider à faire un choix éclairé quant à leur participation à la recherche.
Cela dépend. La fréquence et la durée des visites varie selon le protocole de chaque étude. Vous pouvez avoir des visites mensuelles, trimestrielles, semestrielles ou annuelles.
La durée de chaque visite varie selon le type d’étude. Normalement, les visites pour des études sur les médicaments est plus chargée (1-4h) que celles des études sans traitement (30 min -2 h). Dans la plupart des études, les visites de dépistage ou d’initiation sont plus chargées que les visites de suivi. L’hospitalisation peut parfois s’avérer nécessaire pour une surveillance ou une perfusion plus longue, mais ce cas de figure est rare.
Voici comment se déroulera une visite typique avec un traitement à l’étude:
Test de grossesse et échantillon d’urine
Échantillon de sang
Consultation avec un médecin investigateur
Signes vitaux et autres examens physiques (ex: ECG)
Questionnaire du patient
Administration du traitement
Observation après administration du traitement
Prendre le prochain rendez-vous
La majeure partie de la visite aura lieu dans la section de recherche clinique du service de rhumatologie. Parfois, nous vous demanderons de faire les examens complémentaires dans un autre service de hôpital (radiographie, test pulmonaire, test ophtalmologique …). Parfois, nous pourrons vous demander de remplir un questionnaire chez vous ou de faire une analyse de sang dans un laboratoire local. L’administration du traitement (en particulier pour l’injection sous-cutané) peut être effectuée à votre domicile par une infirmière.
Dans les études à double insu, les participants, les infirmières et les médecins investigateurs ne savent pas quel traitement à l’étude (médicament ou placebo) est utilisé. Seul le pharmacien le sait. Ainsi, les participants et les investigateurs peuvent décrire ce qui se passe en toute objectivité sans être influencé. Cependant, si c’est médicalement nécessaire, il est toujours possible le lever l’aveugle pour savoir ce que le patient prend.
Un placebo est une substance ou un traitement inactif qui ressemble au médicament ou au traitement actif testé. L’effet placebo est l’amélioration réelle ou apparente de l’état du patient sans relation de cause à effet d’un traitement actif sur la maladie. L’utilisation d’un placebo en double aveugle est la méthode de référence permettant d’éviter que l’effet placebo influence et biaise les résultats de la recherche clinique.
C’est le traitement recommandé et habituellement utilisé dans une maladie donnée. Lorsqu’il existe déjà un traitement de référence pour votre maladie, l’essai clinique va comparer un nouveau médicament par-rapport à ce traitement de référence. Lorsqu’il n’existe pas de traitement de référence, l’essai va comparer le nouveau médicament par-rapport au placebo.
Non, sauf en cas d’études sur des volontaires sains. En revanche, certaines études pourront prendre en charge les frais liés à la participation (transport, nourriture, examens supplémentaires…).
Vous êtes libre de changer d’avis et de ne plus participer à l’essai à tout moment et/ou pour quelque raison que ce soit. Communiquez simplement votre décision à votre médecin investigateur. Si votre consentement a été retiré, vos données/échantillons nécessaires à l’étude ne seront plus recueillis. Les données d’ores et déjà recueillies devrons être supprimées et les échantillons détruits. Dans des cas particuliers (condition spécifiée dans la note d’information), les données ou les échantillons recueillis antérieurement à votre retrait de consentement pourront être traités anonymement.
Chaque participant reprend son suivi habituel. Dans certains cas, si les résultats sont positifs, le participant peut participer à une étude complémentaire de suivi et continuer à prendre le traitement à l’étude.
Cela dépend des études. Vous pourrez bien sûr connaître les résultats de l’étude à laquelle vous avez participé et serez directement informé si cela est prévu dans la notice d’information, tout en sachant que ces résultats ne seront parfois connus que des mois, voire des années après votre participation.
Nos principaux projets de recherche "académiques"
Plateforme de médecine personnalisée pour les patients atteints de maladies autoimmunes
L’objectif du projet PERSONALIS est la création d’une base de données contenant des informations anonymes sur les patients atteints de maladies auto-immunes ainsi qu’un outil d’information pour les médecins traitants.
Dans les pays occidentaux, les maladies auto-immunes sont la troisième cause de maladie la plus fréquente et elles touchent particulièrement les jeunes. En raison de leur évolution chronique et souvent invalidante, les effets économiques et sociaux de ces maladies sont également importants. Les immunothérapies ciblées existantes sont souvent inadaptées ou inefficaces.
La base de données vise tout particulièrement à favoriser la stratification biologique des patients, qui est une condition préalable à l’application réussie d’approches thérapeutiques sélectives.
Lien pour le site Offensive science : https://science.rmtmo.eu/actualites/7-laureats-pour-ledition-2018-de-loffensive-sciences-du-rhin-superieur/
Les partenaires sont l’université de Strasbourg (porteur), l’université de Fribourg en Allemagne, l’université de Mayence et la Hochschule für Life Sciences FHNW à Bâle. Partenaires associés: SATT Conectus, EUCOR
– Scleromics
La sclérodermie systémique (SSc) est une maladie rare. Sa prévalence est estimée à 1-9/100 000 pour la sclérodermie localisée et à 1/6500 adultes pour la sclérodermie systémique. La SSc est une maladie dévastatrice caractérisée par des complications viscérales sévères avec une mortalité encore élevée et un impact socio-économique important. A un stade précoce, le diagnostic est difficile car les symptômes sont peu spécifiques à la maladie. Il faudrait chercher des biomarqueurs diagnostiques et pronostiques simples et efficaces, ainsi que des biomarqueurs permettant d’adapter les traitements agressifs.
Le but du projet Scleromics est de créer une cohorte de 140 patients répartis en 5 sous-groupes afin de comparer leur profil métabolomique avec celui de sujets contrôles. Des échantillons de sang, d’urine et de peau sont prélevés et analysés à l’aide d’une technique analytique permettant d’analyser les échantillons à l’échelle moléculaire et de rechercher des signatures « métabolomiques » spécifiques de la maladie (diagnostic précoce) ou de son évolution (médecine prédictive).
Manifestations bucco-dentaires de la sclérodermie systémique : vers la mise en évidence de nouveaux marqueurs pronostiques (étude SclerOral)
La sphère orofaciale est très fréquemment touchée au cours de la sclérodermie systémique avec une variété de manifestations cliniques qui peuvent avoir un impact sur la qualité de vie et nécessitent une prise en charge précoce. Le projet de recherche SclerOral vise à étudier les manifestations bucco-dentaires dans la sclérodermie systémique afin de mettre en évidence des signes cliniques, radiographiques et/ou biologiques spécifiques. Un lien entre certains de ces signes et la sévérité de la maladie pourrait éventuellement être mis en évidence. Par exemple, la présence d’un épaississement du ligament qui entoure les dents (ligament alvéolo-dentaire) constitue un signe radiographique relativement spécifique de la maladie et peut être dans certains cas un des premiers signes radiologiques de la pathologie.
Cette étude se déroule en deux temps. Les patients ont une première visite au Centre de Référence des Maladies Autoimmunes Systémiques Rares Est Sud-Ouest (RESO) au Service d’Immunologie Clinique et de Médecine Interne (Hôpital Civil) ou au Service de Rhumatologie (Hôpital de Hautepierre). La seconde visite se déroule au Centre de référence Maladies Rares Orales et Dentaires (O-Rares) du Pôle de Médecine et de Chirurgie Bucco-dentaires (Hôpital Civil) et comprend un examen bucco-dentaire complet ainsi qu’une radiographie tridimensionnelle du maxillaire et de la mandibule (Cone Beam CT).
Pour plus d’informations, vous pouvez contacter l’investigateur principal du projet : Dr Sophie Jung, Centre de Référence Maladies Rares Orales et Dentaires (O-Rares), sophie.jung1@chru-strasbourg.fr
The European Scleroderma Trials and Research Group (EUSTAR)
C’est un projet qui a pour but d’encourager la reconnaissance, la compréhension et la recherche sur la Sclérodermie Systémique ainsi que sa prise en charge en Europe et dans le reste du monde.
EUSTAR est un réseau de recherche international sur la sclérodermie placé sous l’égide de la Fondation Mondiale pour la Sclérodermie. L’objectif est de coordonner et de concentrer les activités de recherche afin d’améliorer les traitements, la qualité de vie ainsi que le pronostic des patients atteints de sclérodermie. Le réseau EUSTAR, qui a débuté en 2004, était initialement supporté par la Ligue Européenne contre les Rhumatismes (EULAR). L’outil principal de travail est une base de données ou cohorte observationnelle multicentrique internationale qui permet de suivre prospectivement plus de 15 000 patients atteints de sclérodermie dans plus de 200 centres. Chaque patient est vu annuellement lors d’une visite permettant de recueillir des données médicales afin de les analyser.
– SPIRALE
Le lupus érythémateux systémique (LES) est une maladie auto-immune systémique rare. L’évolution de la maladie reste imprévisible pour un patient donné et très peu de biomarqueurs sont disponibles à ce jour pour aider les cliniciens à identifier les patients présentant un risque de poussées. Le fait que la maladie se déclare généralement chez les femmes qui débutent leur vie sexuelle et reproductive, constitue une préoccupation particulière dans le LES car une poussée de la maladie peut avoir des conséquences néfastes sur la mère et sur le développement de l’embryon.
La situation est inversée dans le cas de la Polyarthrite Rhumatoïde (PR), une autre maladie auto-immune systémique, dans laquelle une amélioration marquée, parfois une rémission, peut être observée pendant la grossesse, accompagnée de poussées fréquentes en post-partum.
L’hypothèse émise est la suivante : il existerait des changements épigénétiques spécifiques à la maladie et induits par la grossesse, en particulier ceux qui concernent le schéma et les niveaux de micro-ARN, qui pourraient expliquer le risque de poussées et l’amélioration clinique dans le LES et la PR, respectivement. Dans ce but, 40 patients sont recrutés en subdivisés en 3 groupes (SLE, PR et volontaires sains) et des échantillons biologiques ainsi que des données cliniques sont collectés à différents moments afin d’obtenir l’association entre les modifications induites par la grossesse et le modèle d’expression des micro-ARN.
– ETAP
Le syndrome de Sjögren primitif est une maladie rare, concernant environ 0.1% de la population. Cette maladie auto-immune systémique se caractérise par une sécheresse de l’ensemble des muqueuses, une grande asthénie, des douleurs diffuses chez la majorité des patients et des complications systémiques chez 30% des malades. Aucun traitement n’a réellement prouvé son efficacité aujourd’hui dans cette maladie. Actuellement, le Tocilizumab (TCZ) semble être un bon candidat dans cette maladie en raison du rôle pathogène démontré de l’IL-6 au cours de la pathologie.
Dans le cadre de ce projet, 110 patients sont recrutés en deux groupes (patients recevant du TCZ ou un placebo) dans le but d’évaluer l’efficacité et la tolérance du TCZ.
– RTU
La maladie de Takayasu est une maladie rare qui touche l’aorte et ses principales ramifications. Son incidence est estimée à 3/100 000 personnes. La prise en charge de cette pathologie n’est pas clairement codifiée à ce jour. Une recommandation temporaire d’utilisation (RTU) est un dispositif d’encadrement transitoire qui permet, en France, l’utilisation de certains médicaments en dehors de leur autorisation de mise sur le marché (AMM). Une RTU a été établie en octobre 2017 par l’Agence Nationale de la Santé et du Médicament pour évaluer le rapport bénéfice/risque dans cette population ayant un besoin thérapeutique. Dans le cadre de cette RTU, les médecins spécialistes peuvent prescrire de l’Infliximab aux patients atteints de la maladie de Takayasu et qui sont réfractaires aux traitements conventionnels en respectant un protocole de suivi. Ce protocole permet le recueil des données sur l’efficacité et la sécurité du traitement. L’ensemble des données collectées ont été analysées et transmises à l’ANSM.
– Rarenet
C’est un projet de coopération transfrontalière franco-germano-suisse qui a pour but d’améliorer la prise en charge et la santé de personnes atteintes d’une maladie rare ou complexe. Le réseau RARENET rassemble des chercheurs, des praticiens et des associations de patients et, ensemble, ils travaillent autour de deux formes de pathologies : les anomalies bucco-dentaires provoquées par ces maladies et les maladies auto-immunes.
Ce projet s’attache à constituer une vaste cohorte de patients avec réalisation d’une banque de sérum et d’ADN notamment. L’intérêt d’une telle cohorte est de réunir suffisamment de patients se ressemblant dans un ensemble hétérogène pour essayer de repérer des points communs ou des mécanismes communs de la maladie en étudiant l’histoire clinique et les échantillons biologiques de ces patients.
ISLE Study :
L’accélération du phénomène d’athérosclérose est une complication établie des maladies auto-immunes systémiques, et particulièrement le lupus érythémateux systémique (LES). Les patients atteints de LES sont plus susceptibles de développer un infarctus du myocarde que des témoins appariés, et les maladies cardio-vasculaires constituent la cause majeure de décès pour les patients LES (27%). L’objectif de cette étude est d’évaluer la fiabilité, la valeur prédictive et l’utilité de biomarqueurs immunologiques dans la stratification du risque cardiovasculaire dans le LES , à partir d’une cohorte prospective européenne avec collection d’échantillons biologiques associée. L’objectif principal est d’estimer la prévalence de patients qui présentent une plaque d’athérosclérose ou une progression du diamètre intima-media carotidien après 18 mois de suivi. Chaque patient remplira les auto-questionnaires validés d’alimentation et de l’activité physique pour évaluer son risque cardiovasculaire. Une échographie permettra une évaluation de plaques d’athérosclérose et l’épaisseur de la carotide intima-média. Cet examen sera effectué le jour de l’inclusion et après 18 mois de suivi ainsi que des prélèvements sanguins permettant la constitution d’une collection d’ échantillons biologiques.
ImmunAID :
Les MAIS (Maladies Auto Immunes Systémiques) rares constituent un ensemble de maladies qui peuvent être héréditaires et aux symptômes peu spécifiques (fièvres, éruption cutanées, douleurs articulaires…) et qui présentent des similitudes phénotypiques. Ces maladies peuvent être divisées en deux groupes :
– Les maladies monogéniques auto-inflammatoires pour lesquelles des mutations ont été identifiées : fièvre méditerranéenne familiale ou maladie périodique (FMF), syndrome périodique associé au récepteur du TNF (TRAPS), syndrome hyper-IgD ou déficit partiel en mévalonate kinase (HIDS), syndrome périodique associé aux cryopyrinopathies ou urticaire familiale au froid (CAPS)
– Les maladies dites génétiquement indéterminées pour lesquelles aucune mutation génétique n’a été identifiée et pour lesquelles le diagnostic repose sur l’élimination de toute autre cause de maladie : Maladie de Still, péricardite récurrente, dermatose neutrophilique, syndrôme de Schnitzler, vascularites, inflammation d’origine inconnue et ostéite chronique de l’enfant ou de l’adulte.
A l’heure actuelle les causes et mécanismes de ces maladies sont mal connues et leur diagnostic est difficile et long, entrainant souvent des erreurs de diagnostic.
L’objectif de l’étude « ImmunAID » est la collecte des données cliniques ainsi que des échantillons biologiques dérivés du sang (plasma, sérum, cellules et ADN), de l’urine et des selles pour des analyses biologiques multi-omiques et fonctionnelles seront analysées au moyen de méthodes bio-informatiques, statistiques et de « machine learning » et aboutiront à l’élaboration d’algorithmes de classification diagnostique (signatures) pour les MAIS.
Grâce à des analyses parallèles effectuées sur des échantillons de 1616 patients atteints de MAIS monogéniques ou génétiquement indéterminées, parents de patients ou contrôles négatifs, collectés dans toute l’Europe, le projet du consortium ImmunAID produira un ensemble unique et complet de données. Dans l’ensemble, ImmunAID démêlera le spectre des MAIS et proposera une nouvelle classification basée sur l’omique et la pathogenèse, associée à un algorithme de prise de décision clinique pouvant être mis en œuvre dans la pratique quotidienne.
EFIRTES
La sarcoïdose est une maladie granulomateuse multisystémique de cause inconnue . La sarcoïdose est chronique et progressiste chez 25 % des patients. Bien que les ganglions lymphatiques médiastinaux et les poumons soient les sites les plus fréquemment touchés, des localisations extra-thoraciques peuvent se produire. En particulier, les localisations cardiaques ou neurologiques sont fréquemment associées à une maladie chronique, avec morbidité et mortalité subséquentes . Ces patients nécessitent un traitement à long terme pour éviter un dysfonctionnement des organes qui peut survenir avec la fibrose. Les corticostéroïdes sont le médicament de choix pour ces localisations, mais des toxicités cumulatives peuvent survenir. Le méthotrexate, l’azathioprine et le mycophénolate peuvent être utilisés comme stéroïdes de première ligne. En cas de corticorésistance ou de dépendance à une dose journalière de stéroïdes supérieure à 10 mg/j, des immunosuppresseurs secondaires peuvent être utilisés . Récemment, l’infliximab, un anticorps monoclonal chimérique de l’immunoglobuline G dirigé contre le TNF-alpha, a montré une efficacité chez les patients atteints de sarcoïdoses pulmonaires. Comme l’infliximab a démontré une réelle efficacité dans la sarcoïdose résistante, nous supposons qu’il pourrait être une option précieuse pour l’induction de la rémission dans les sarcoïdoses extra-thoraciques sévères. La durée de participation varie de 16 à 22 semaines.
MAINESPAN
Le traitement immunosuppresseur de la granulomatose avec polyangéite (GPA, anciennement maladie de Wegener) et de la polyangéite microscopique (PAM) a diminué la mortalité et permis une forte proportion de rémission temporaire de la maladie. Cependant, la plupart des patients présentent des rechutes entrainant des séquelles. Ces rechutes nécessitent un traitement répété et sont associées à une augmentation de la morbidité à long terme et à une surmortalité. Le rituximab s’est avéré aussi efficace que le cyclophosphamide pour induire la rémission et le maintien de la rémission chez des patients atteints de GPA et PAM sévères, avec un profil de sécurité acceptable. Cependant, bien que le rituximab devienne le traitement standard d’entretien chez ces patients, les rechutes sont encore fréquentes et la durée optimale de la corticothérapie d’entretien par la prednisone reste débattue. L’essai clinique MAINESPAN est le premier essai prospectif évaluant le maintien de la rémission par utilisation prolongée de prednisone chez des patients atteints de vascularites associées aux anticorps cytoplasmiques anti-neutrophiles systémiques (ANCA)
