
Focus sur une pathologie
LUPUS SYSTEMIQUE
Le Lupus Erythémateux Systémique (LES) est une maladie auto-immune caractérisée par l’association de manifestations très diverses et par la présence d’anticorps dirigés contre divers constituants du noyau (les anticorps antinucléaires). La maladie est mieux connue du grand public depuis que Selena Gomez a annoncé qu’elle était atteinte de ce diagnostic et avait même bénéficié d’une transplantation rénale. Le LES est une maladie chronique qui appartient au groupe des connectivites et dont le pronostic s’est considérablement amélioré au cours des dernières décennies (l’espérance de vie dépasse 95% à 10 ans dans la plupart des centres spécialisés). L’objectif thérapeutique à court terme est le traitement des poussées ; à moyen et long terme, la prévention des rechutes en essayant de limiter les séquelles de la maladie et les effets délétères des traitements tout en maintenant la qualité de vie la plus optimale possible. En France, environ 30 000 personnes sont atteintes par le lupus systémique.
épidemiologie
du lupus systémique
L'histoire
du lupus systEmique
Découvrez l’histoire du mot « lupus » à travers les siècles, racontée (en anglais) par le Pr Laurent ARNAUD (CRMR RESO)
Symptômes du lupus systemique
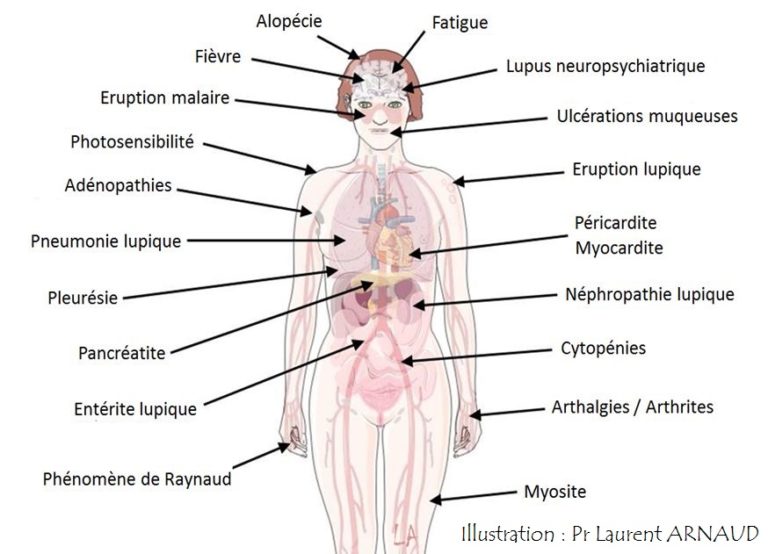
Les symptômes du lupus systémique sont ceux d'une maladie très polymorphe
Les symptômes du lupus sont très variés pendant les poussées et les patients peuvent présenter de nombreuses manifestations en dehors du masque de loup.
Des signes généraux sont présents dans 30 à 50% des cas au cours des poussées. Ils sont non spécifiques, à type de fièvre (parfois élevée) non infectieuse, et peuvent s’associer à un amaigrissement, ou encore à une asthénie (très fréquente). Une polyadénopathie est fréquente au cours des poussées, mais non spécifique.
Atteinte cutanée et muqueuse
L’atteinte cutanéo-muqueuse est présente dans 75 à 80% des cas, et inaugurale dans 20 à 25% des cas. Les atteintes cutanées spécifiques peuvent être à type de lupus aigu, subaigu ou chronique. La photosensibilité est un élément classiquement retrouvé (≈40-50% des cas).
Lupus aigu
Le lupus aigu se caractérise par un érythème maculo-papuleux à bordure émiettée, avec une topographie en vespertilio (érythème malaire) ou touchant le décolleté, ou le dos des mains. L’évolution spontanée se fait par poussées, sans séquelles cicatricielles entre les poussées.
Lupus subaigu
Le lupus subaigu se caractérise par des lésions annulaires, polycycliques, parfois télangiectasiques ou psoriasiforme. Elle prédomine également dans les zones photo-exposées.
Atteintes chroniques
Ces atteintes comportent notamment le lupus discoïde, qui correspond à des lésions érythémato-squameuses, avec une évolution atrophique et cicatricielle définitive, ce qui fait toute sa gravité en raison du préjudice esthétique.
Autres atteintes cutanéo-muqueuses
Les autres atteintes décrites sont l’alopécie, le purpura, le livedo, l’urticaire, les ulcérations bucco-pharyngées, les télangiectasies péri-unguéales ou les hémorragies sous-unguéales.
Atteintes rhumatologiques
Atteinte articulaire
L’atteinte articulaire est très fréquente (≈60-80% des patients) et souvent révélatrice. Il s’agit principalement d’arthralgies, et moins fréquemment d’arthrites ou de ténosynovites. L’horaire des douleurs est inflammatoire (réveils nocturnes, persistance matinale > 30 minutes, non améliorées par le repos). L’atteinte est le plus souvent bilatérale et symétrique, et prédomine généralement aux doigts, mains et poignets, mais peut toucher toutes les articulations. Le plus souvent, le lupus n’entraine pas de déformation. Cependant, il peut rarement s’y associer une déformation réductible des mains (rhumatisme de Jaccoud) mais il n’y a alors classiquement pas d’érosion articulaire radiographique, telle qu’on pourrait l’observer dans la polyarthrite rhumatoïde.
Atteinte osseuse et musculaire
Une atteinte musculaire (myalgies, déficit musculaire, amyotrophie) est rare mais possible, notamment dans le cadre d’un syndrome de chevauchement avec d’autres connectivites. Une atteinte musculaire peut également se voir dans le cadre d’une myopathie cortisonée, qui est une des atteintes iatrogènes pouvant se surajouter aux atteintes propres à la maladie. Des douleurs des hanches, des épaules, des genoux ou du rachis doivent également faire suspecter des ostéonécroses (généralement en rapport avec la corticothérapie ou la présence d’anticorps anti-phospholipides) ou des complications fracturaires.
Atteintes cardio-pulmonaires
Les sérites
La péricardite lupique doit être évoquée devant des douleurs thoraciques, mais peut être asymptomatique. Elle concerne 18 à 40% des lupiques. Le risque d’évolution vers la tamponnade est possible mais rare.
La pleurésie lupique est généralement bilatérale, de type exsudative lymphocytaire, et concerne 30 à 40% des lupiques.
Autres atteintes cardiaques
La myocardite : dont l’expression peut prendre la forme d’une insuffisance cardiaque, de troubles du rythme ou de la conduction.
L’endocardite de Libman-Sacks : il s’agit d’une endocardite fibrino-crurotique, non infectieuse, associée à la présence d’anticorps anti-phospholipides. Sa prise en charge nécessite une anticoagulation à dose curative en raison d’un fort risque d’embolisation artériel.
Autres atteintes pulmonaires
L’atteinte pulmonaire parenchymateuse, responsable de fibrose interstitielle ou se manifestant par une hémorragie intra-alvéolaire est rare : le lupus est l’une des rares connectivites qui ne touche pas fréquemment le poumon.
L’hypertension artérielle pulmonaire, dont la survenue grève sévèrement le pronostic de la maladie doit être évoquée devant une dyspnée ou des syncopes d’effort.
Atteintes vasculaires
Phénomène de Raynaud
Il est présent chez 10 à 30% des patients lupiques. Contrairement à la sclérodermie systémique, celui-ci est rarement compliqué de troubles trophiques.
Syndrome des anti-phospholipides (SAPL)
Le syndrome des anti phospholipides, est une étiologie de thrombophilie fréquemment associée au lupus (≈40% des cas), bien qu’il puisse exister de manière totalement indépendante (SAPL primaire). Le SAPL est responsable de complications thrombotiques veineuses, notamment dans des territoires atypiques (embolie pulmonaire et thromboses veineuses profondes multiples et récidivantes, notamment des membres inférieurs, mais aussi de la veine porte, des veines sus-hépatiques, ou des sinus veineux cérébraux). Il se manifeste aussi par des thromboses artérielles (AVC, infarctus du myocarde, ischémie de membre, ischémie mésentérique). Il s’y associe des complications obstétricales (fausses couches précoces ou tardives,
pré-éclampsie/éclampsie.) Il existe un consensus international sur les critères de classification du SAPL (2006).
Atteinte néphrologique
Un véritable enjeu diagnostique
L’atteinte rénale est l’un des principaux déterminants du pronostic de la maladie. Elle est inaugurale dans 3 à 6% des cas, et elle sera présente chez 30 à 75 % des patients lupiques au cours du suivi. Son dépistage doit être réalisé à chaque consultation, y compris en l’absence de signes cliniques (une atteinte rénale sévère peut évoluer sur plusieurs mois, sans
expression clinique bruyante). Il s’agit généralement d’une atteinte glomérulaire, bien que des atteintes tubulo-interstitielles ou vasculaires soient parfois observées. L’atteinte rénale se manifeste par une protéinurie en général > 500mg/24h (c’est-à-dire un ratio >50mg/mmol), parfois associée à une hématurie microscopique. Il peut s’y associer une hypertension artérielle, des œdèmes et/ ou une altération de la fonction rénale. L’atteinte rénale peut être isolée, et ne s’accompagne donc pas forcément d’autres atteintes cliniques du lupus. Le risque, en l’absence de prise en charge précoce et appropriée, est d’aboutir à une insuffisance rénale terminale (actuellement ≈10% des patients avec atteinte rénale), avec la nécessité d’hémodialyse et/ou d’une transplantation rénale.
Comment diagnostiquer l’atteinte rénale du lupus
Le dépistage repose sur la bandelette urinaire à chaque visite puis, en cas de positivité, la réalisation d’une protéinurie des 24h (ou d’une mesure du ratio protéinurie sur créatininurie), d’un sédiment urinaire, et d’un ECBU. En cas de protéinurie supérieure à 0,5g/24h, les patients doivent être adressés rapidement en consultation spécialisée afin de discuter la réalisation d’une ponction biopsie rénale (les patients ayant une protéinurie positive, mais <0,5g/24h doivent bénéficier d’un contrôle mensuel de la protéinurie car celle-ci peut rapidement augmenter).
L’analyse de la biopsie rénale permet de classer le type d’atteinte, et de savoir s’il s’agit de lésions actives (accessibles à un traitement) ou de lésions fibreuses séquellaires (irréversibles). Il existe une classification histologique des néphropathies glomérulaires lupiques. La classe identifiée à la biopsie rénale permettra de conditionner le protocole de prise en charge thérapeutique ; celle-ci est donc indispensable.
Atteintes neurologiques
Atteinte du système nerveux central (SNC)
L’expression clinique du « neuro-lupus » est extrêmement variable, avec notamment des crises convulsives, pouvant être généralisées ou focales, de chorée, d’atteintes vasculaires notamment dans le cadre du SAPL (l’atteinte est soit artérielle, avec une symptomatologie d’AVC, soit il peut s’agir de thromboses veineuses cérébrales avec un tableau clinique de céphalées
intenses et persistantes, et/ou des signes focaux ou déficitaires). L’atteinte peut concerner la totalité du système nerveux, y compris la moelle. Parfois il s’agit de troubles cognitifs (mnésiques), ou de désordres psychiatriques avec des troubles du comportement, des troubles de l’humeur, voire un véritable tableau délirant. Il peut s’agit de céphalées (rarement), parfois invalidantes, avec critères de migraines ou non, mais devant par définition résister aux antalgiques majeurs pour pouvoir entrer
dans le cadre de la définition des céphalées lupique. Une céphalée brutale doit d’abord et avant tout faire rechercher une cause vasculaire et ou infectieuse en urgence.
Autres atteintes neurologiques
Il peut s’agir de méningites aseptiques lymphocytaires, mais également de neuropathies (polyradiculonévrite, neuropathie végétative, etc…).
diagnostic du lupus systemique
Les examens biologiques de routine
Le syndrome inflammatoire biologique
Il est marqué par l’élévation de la vitesse de sédimentation (VS), à laquelle s’associe souvent une hypergammaglobulinémie polyclonale avec une élévation des alpha-2 globulines à l’électrophorèse des protéines plasmatiques. Il y a fréquemment une dissociation entre la VS et la C-réactive protéine, avec une élévation moins marquée de la CRP par rapport aux autres marqueurs de l’inflammation biologique (la CRP est le plus souvent normale ou sub-normale au cours du lupus, sauf aux cours des sérites et de certaines complications rares). Une CRP élevée doit donc faire avant tout suspecter une problématique infectieuse avant d’attribuer le syndrome inflammatoire à une poussée lupique.
Atteintes hématologiques : cytopénies
Anémie
En pratique, l’anémie peut-être multifactorielle : périphérique et régénérative par origine hémolytique auto-immune (le test de Coombs est alors positif) ou mécanique (présence de schizocytes), ou centrale, et alors non régénérative, secondaire à l’inflammation chronique ou une atteinte médullaire. Parfois cette anémie est majorée par la présence d’une insuffisance rénale avec une insuffisance de sécrétion d’érythropoïétine (EPO). Dans de rares cas, un troisième mécanisme peut survenir : il s’agit d’une anémie centrale non régénérative d’origine auto-immune avec des anticorps dirigés contre les progéniteurs médullaires des réticulocytes (érythroblastopénie).
Thrombopénie
La thrombopénie est en générale d’origine périphérique, par hyper-destruction des plaquettes médiée par un mécanisme auto-immun (anticorps anti-plaquettes). L’association thrombopénie et anémie auto-immune définit le syndrome d’Evans. Les patients ayant une thrombopénie <50 000 plaquettes/mm3 doivent être adressés rapidement en milieu spécialisé.
Leucopénie
Chez la plupart des patients lupiques, il existe une diminution modérée du nombre de leucocytes, généralement entre 2000 et 4000/mm3, et notamment une lymphopénie inférieure à 1000/mm3, qui est très fréquente. Les atteintes des lignées blanches peuvent être d’origine iatrogène médicamenteuse.
Dosage du complément sérique
Le dosage des protéines du complément sérique peut être abaissé dans le lupus, notamment lorsque il existe une forte activité de la maladie ou plus rarement un déficit génétique constitutionnel (cet abaissement du CH50, du C3 ou du C4 est donc très inconstant, et un dosage de complément normal ne permet pas d’éliminer la possibilité d’un lupus). Le dosage du C3 est utile au cours du suivi pour apprécier l’évolutivité globale de la maladie.
Les auto-anticorps du lupus systémique
Les anticorps antinucléaires
Sauf situation exceptionnelle, la totalité des patients lupiques présentent une positivité des anticorps anti-nucléaires (titre ≥ 1/80ème), qui sont recherchés par des techniques d’immunofluorescence indirecte. La recherche des FAN doit être demandée devant toute suspicion de lupus, et la négativité de cette recherche est un argument très fort contre le diagnostic de lupus.
Les anticorps anti-ADN natif (=ADN double brin)
En cas de positivité des anticorps anti nucléaires, la recherche d’anti ADN natif (= anti ADN double brin) peut être demandée en cas de suspicion de lupus. Leur identification dans le sérum des patients est précieux car ils sont beaucoup plus spécifiques du lupus (bien que moins sensibles) : 60 à 80% des patients lupiques sont concernés. Leur taux est corrélé à l’activité de la maladie et relativement prédictif de la survenue d’une atteinte rénale.
Les autres auto-anticorps
• Anticorps anti-histone : ils ont surtout été décrits au cours du lupus induit par les médicaments. Leur dosage ne doit pas être fait en routine et reste réservé à une prise en charge spécialisée, leur valeur diagnostique étant contestée.
Les anticorps anti-Sm : très spécifiques du lupus, mais présents dans seulement 10 à 30% des cas. En cas de positivité, leur présence est un argument très fort en faveur du diagnostic de lupus systémique.
D’autres anticorps, fréquemment retrouvés au cours du lupus, sont les anti-SSA et anti-SSB (également retrouvés au cours du syndrome de Sjögren), et anti-RNP (également retrouvés au cours de la connectivite mixte).
causes du lupus systémique
Implication du système immunitaire
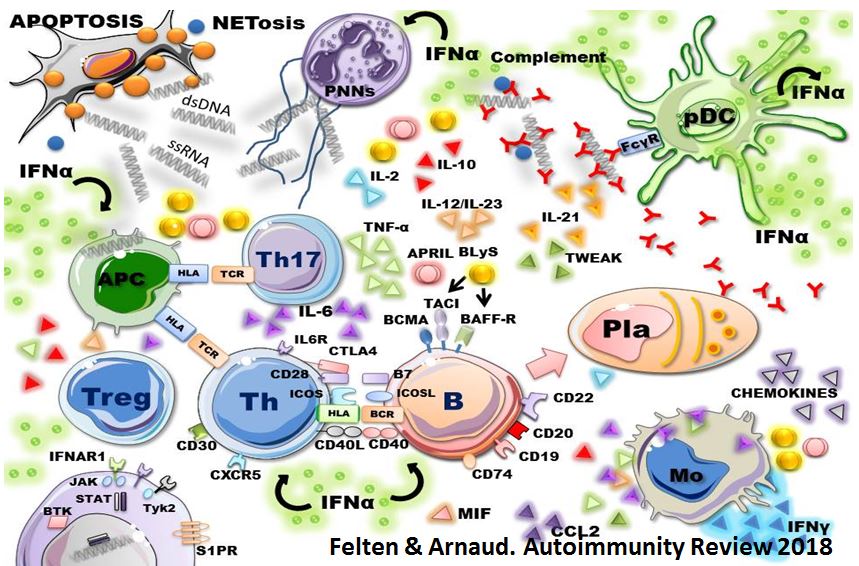
La pathogénie du lupus systémique est particulièrement complexe, et fait appel à la production d’anticorps dirigés contre certains constituants du noyau cellulaire (anticorps anti-nucléaires), qui vont former des complexes immuns avec les antigènes nucléaires libérés lors de l’apoptose accrue des cellules (par exemple sous l’influence des rayons ultraviolets). Ces complexes immuns vont activer certaines molécules (dont les voies du complément, qui sera consommé) et des cellules spécialisées, telles que les cellules dendritiques plasmacytoïdes (pDC), qui vont libérer de grandes quantité d’interféron (en particulier interféron alpha) qui va booster l’activité du système immunitaire.
traitement du lupus systemique
Objectifs du traitement
L’objectif du traitement correspond à une prise en charge globale, pluridisciplinaire, qui doit être mise en place sur le long terme. L’objectif est de préserver les fonctions nobles, et de prévenir les poussées de la maladie, notamment de prévenir les poussées avec une atteinte d’organe sévère engageant le pronostic vital (cardio-pulmonaire, néphrologique, neurologique, vasculaire). Mais l’objectif est également de réduire le handicap fonctionnel (atteinte cutanée, rhumatologique) afin d’éviter le retentissement social, professionnel, familial et psychologique lié à l’activité de la maladie ou de ses séquelles. Cette finalité a pour but d’améliorer et de préserver la qualité de vie des patients lupiques.
Traitement non médicamenteux
Education therapeutique
Il s’agit d’une maladie chronique, évoluant par poussées entrecoupées de périodes de rémission durant lesquelles la maladie est quiescente. L’éducation thérapeutique reste une nécessité pour assurer une compréhension de la maladie et aborder l’importance de l’observance des traitements.
Photoprotection
L’application d’écran solaire d’indice de protection maximal est obligatoire, et doit être associée à des vêtements adaptés afin d’éviter la survenue de lésions photo-induites ou de déclencher des poussées lupiques par l’exposition solaire.
Risque infectieux
Elle repose sur la mise à jour des vaccinations et le suivi du carnet vaccinal, notamment avec la vaccination antipneumococcique (recommandée chez tous les patients lupiques) et antigrippale saisonnière (recommandée chez les patients lupiques sous immunosuppresseurs) : le médecin généraliste à un rôle majeur dans le suivi des patients
Risque cardiovasculaire
La présence d’une inflammation chronique, d’une poly-médication (dont la corticothérapie), ou d’un tabagisme actif, augmente fortement le risque cardio vasculaire global, avec une diminution de l’espérance de vie des patients lupiques par rapport à la population générale. Ceci rend nécessaire le suivi rapproché et efficace des comorbidités, avec un contrôle rigoureux des facteurs de risque cardiovasculaires. Cela peut passer par un suivi régulier chez une cardiologue, même en l’absence d’atteinte cardiaque lupique propre. Le respect des règles hygiéno-diététiques et le sevrage tabagique sont primordiaux.
Suivi gynécologique
Il y a une nécessité d’une contraception orale par pillule microprogestative ou d’une contraception mécanique chez les femmes lupiques, avec une contre-indication des oestro-progestatifs, connus pour aggraver la maladie. La grossesse est tout à fait possible au cours du lupus, mais dans la mesure où elle peut aggraver la maladie, elle ne doit s’envisager qu’avec un encadrement médical spécialisé, et à distance de toute poussée (chez une patiente dont la maladie est bien contrôlée depuis plus de 6 mois).
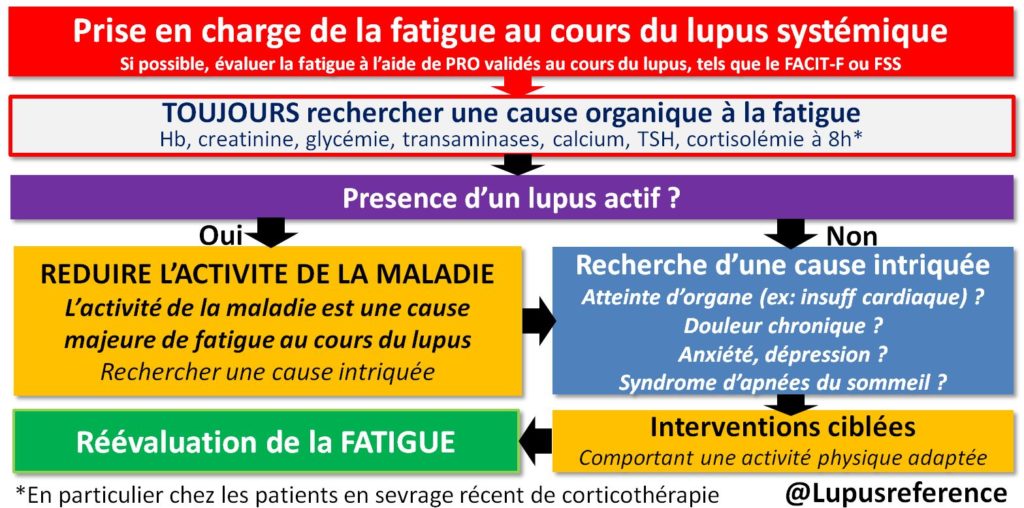
Prise en charge diagnostique et thérapeutique de la fatigue au cours du lupus
Les traitements médicamenteux du lupus systémique
La corticothérapie
Elle est souvent nécessaire en cas de poussée grave ou sévère, parfois même par voie intraveineuse. La posologie de corticoïdes doit être déterminée par un spécialiste du lupus. En cas de poussée articulaire isolée, la majorité des patients répondent à des doses de prednisone de l’ordre de 10 à 15mg par jour, et il n’est généralement pas nécessaire d’utiliser des doses plus élevées). Les anti-inflammatoires non stéroïdiens en cure courte peuvent également être utilisés en cas d’atteinte articulaire (sauf l’ibuprofène, qui est contre-indiqué au cours du lupus en raison du risque de méningite aseptique).A distance des poussées, l’objectif est une décroissance progressive. La prise en charge des effets secondaires cortico-induits doit s’y associer : le respect d’un régime pauvre en sel et en sucres rapides, la supplémentation en calcium et en vitamine D, avec une prévention de l’ostéoporose cortico-induite par un bisphosphonate. L’objectif est de maintenir une activité physique et de respecter les règles hygiéno-diététiques pour éviter les effets secondaires endocrino-métaboliques délétères au long cours. Cela nécessite le dépistage et le traitement des foyers infectieux potentiels, notamment urinaires ou dentaires.
Les antimalariques (hydroxychloroquine)
Il s’agit de l’hydroxychloroquine, qui est un traitement immunomodulateur et non immunosuppresseur (pas d’augmentation du risque d’infection). Sauf contre-indication (allergie, rétinopathie), tous les patients lupiques doivent bénéficier d’un traitement par hydroxychloroquine. Ce traitement suffit en général dans les formes « bénignes » cutanéo-articulaires peu sévères. Mais l’antipaludéen à toute sa place dans les formes sévères également, au long cours. L’objectif est le maintien d’une dose de 400mg/j en deux prises, avec un contrôle de l’observance possible par dosage des taux sériques d’hydroxychloroquine. Le plus souvent, il faut y organiser un suivi ophtalmologique spécifique au cours de la première année puis annuel à partir de la 5ème année de traitement pour ne pas méconnaitre un effet secondaire rare mais imposant son arrêt : la rétinopathie aux antipaludéens.
Les immunosuppresseurs et biothérapies
Ils sont nécessaires dans les formes graves, c’est à dire engageant le pronostic vital ou à risque de séquelles viscérales définitives, ou à visée d’épargne cortisonique. Leur initiation est hospitalière et se fait dans des services spécialisés.Dans les formes articulaires persistantes, le méthotrexate hebdomadaire est parfois proposé.Le cyclophosphamide intraveineux en perfusion mensuelle ou bimensuelle. Il est cytotoxique pour la vessie, raison pour laquelle un traitement par MESNA est associé. Actuellement dans certaines formes, sont également utilisé des biothérapies telles que le Rituximab (hors AMM), ou le Belimumab en perfusions ou injections sous-cutanées.
LUPUS SYSTEMIQUE
Les challenges du lupus systemique
Découvrez les principaux challenges (en anglais) dans le diagnostic, le suivi, et le traitement du lupus systémique, par le Professeur Laurent ARNAUD (CRMR RESO)
LUPUS SYSTEMIQUE
LA RECHERCHE SUR LE LUPUS AU CENTRE DE REFERENCE DE STRASBOURG
De nouveaux traitements du lupus sont en cours d’étude. La recherche est très active dans le domaine du syndrome de lupus et de nouveaux patients participent aux essais cliniques, ce qui donne l’espoir de trouver des traitements plus adaptés à l’avenir. Le centre de référence de Strasbourg est particulièrement impliqué dans cette activité de recherche :
1) Le centre de référence de Strasbourg a un rôle moteur dans l’évaluation de différentes stratégies médicamenteuses au cours du lupus
2) Le centre de référence de Strasbourg coordonne plusieurs essais cliniques de médicament au cours du lupus
3) Le centre de référence de Strasbourg coordonne pour la France également l’étude SPOCS qui suit, à long terme des patients atteints de lupus pour évaluer le lien entre les traitements et la signature interféron et participe à de nombreux essais cliniques académiques ou promus par l’industrie pharmaceutique
4) Le centre de référence de Strasbourg participe à de nombreux groupe de recherche et sociétés savantes autour du lupus : SLICC, DORIS, ERN-RECONNET, SLEeuro, etc.
5) Le centre de référence de Strasbourg coordonne de nombreuses études autour de l’épidémiologie du lupus systémique, en particulier dans les bases de l’assurance maladie, etc, ainsi que sur le rôle des facteurs environnementaux.
LUPUS SYSTEMIQUE
