
Focus sur une pathologie
POLYCHONDRITE
CHRONIQUE
ATROPHIANTE
La polychondrite chronique atrophiante (PCA) est une maladie systémique rare, touchant principalement les cartilages des oreilles, du nez et de l’arbre respiratoires, mais qui peut également atteindre d’autres organes en particulier les yeux, la peau, les articulations, le système cardiovasculaire, les lignées sanguines. Compte tenu de la rareté de la pathologie et de la complexité de la prise en charge, le suivi des patients atteints de PCA doit idéalement être réalisé dans le cadre d’un centre national de référence tel que celui de Strasbourg.
épidemiologie de LA POLYCHONDRITE
symptômes de la polychondrite
Environ 1/3 des PCA sont révélées par des chondrites, dont la présence est indispensable au diagnostic. Le tableau clinique habituel associe donc des chondrites à d’autres atteintes tissulaires ou d’organe, de fréquence variable, ainsi qu’une atteinte variable de l’état général. L’évolution de la maladie est marquée par des poussées plus ou moins fréquentes, et sa sévérité est variable d’un patient à un autre. Cependant, la plupart des patients présentent une forme marquée de la maladie, avec des poussées parfois répétées et invalidantes, mettant en jeu le pronostic fonctionnel voire vital. Les formes mineures sont quant à elles relativement rares.
Signes généraux
Fatigue et asthénie sont des manifestations fréquentes au cours de la PCA, pouvant persister en dehors de tout signe d’activité clinique. Une fièvre peut être observée, devant faire évoquer en premier lieu un processus infectieux ou (para)néoplasique.
Chondrites auriculaires
L’atteinte la plus fréquente et la plus évocatrice de la maladie est la chondrite du pavillon de l’oreille (≈85% des patients au cours de l’évolution de la maladie). Cette chondrite peut être uni ou bilatérale, et se traduit par une douleur importante, avec rougeur et tuméfaction du pavillon de l’oreille. Un point essentiel est que cette inflammation épargne le lobule de l’oreille, de nature non cartilagineuse (figure 1). Elle évolue de quelques jours à quelques semaines et peut régresser spontanément.
Elle peut être responsable de la destruction du cartilage auriculaire (« oreilles de cocker »), ou à l’opposé d’un épaississement et une déformation avec parfois des calcifications du cartilage responsable d’une déformation typique appelée « oreille en chou-fleur ».
Il est indispensable d’examiner également le conduit auditif externe, qui peut être obstrué par un œdème inflammatoire ou par un collapsus du cartilage secondaire à une chondrite de la trompe d’Eustache ou à une otite séreuse moyenne entrainant une surdité de transmission.
L’oreille interne peut également être touchée, entrainant une surdité de perception et/ou des vertiges avec syndrome vestibulaire (≈1/3 des patients).
Chondrites nasales
La chondrite nasale est moins fréquente que la chondrite auriculaire (50-65% des patients selon les séries). Dans la forme la plus bruyante, le patient ressent une douleur au niveau de la racine du nez, zone de jonction entre os et cartilage nasal, sans aucun signe inflammatoire local. La répétition des poussées inflammatoires nasales peut aboutir à une destruction du cartilage avec apparition d’une déformation typique mais non spécifique appelée « nez en pied de marmite », observée chez environ 20% des patients pendant l’évolution de la maladie. Il n’est pas rare d’avoir une déformation sans chondrite symptomatique.
Chondrites des voies aériennes
La chondrite de l’arbre respiratoire est une cause importante de morbi-mortalité au cours de la PCA. Elle touche environ 50% des patients au cours de l’évolution de la maladie. Elle signe un phénotype grave de cette maladie, et indique un traitement précoce et intensif pour limiter l’apparition de séquelles importantes. L’hospitalisation en réanimation devant un tableau de détresse respiratoire aigüe n’est pas rare.
L’atteinte laryngée se manifeste par une toux sèche, avec dysphonie voire aphonie secondaire à l’œdème +/- paralysie des cordes vocales. Peuvent s’y associer une dyspnée laryngée, des cervicalgies antérieures aggravées par la palpation des structures cartilagineuses superficielles ou plus rarement un stridor en cas de sténose sous-glottique. Ces atteintes peuvent évoluer vers des tableaux de détresse respiratoire.
L’atteinte trachéo-bronchique est la plus grave. Sa recherche doit être systématique devant toute suspicion de PCA. Elle doit être évoquée devant une toux sèche, une dyspnée, un asthme inhabituel ou atypique et parfois un wheezing. Cette atteinte peut aboutir au collapsus trachéo-bronchique et/ou au rétrécissement de la lumière par épaississement œdémateux des parois bronchiques aboutissant à des tableaux d’insuffisance respiratoire nécessitant parfois le recours à la chirurgie reconstructrice. La portion membraneuse postérieure est en général épargnée sauf dans les formes évoluées où l’épaississement peut être circonférentiel.
L’atteinte des grosses voies aériennes se complique fréquemment d’atélectasie et/ou d’infections bactériennes. Les indications aux endoscopies, biopsies ou intubations doivent être mûrement réfléchies dans la mesure où il existe un risque accru de perforation ou de déclenchement d’une poussée en cas de geste invasif.
Une fibrose pulmonaire est observée exceptionnellement, et l’on ne sait pas s’il s’agit d’une manifestation de la maladie ou d’une association.
Chondrite costo-sternale
Les chondrites costales se manifestent par des douleurs de la paroi thoracique antérieure et/ou des côtes flottantes, reproductibles à la palpation et parfois accompagnées de phénomènes inflammatoires locaux. Ces atteintes sont très évocatrices de la maladie, et doivent être évoquées devant des manifestations évoquant un syndrome de Tietze à symptomatologie récidivante.
La chondrite costale et/ou la douleur qu’elle entraine est fréquemment responsable d’un trouble ventilatoire restrictif.
Atteinte articulaire et musculaire
Les manifestations articulaires sont parmi les plus fréquentes de la PCA (≈65% des malades) et fréquemment révélatrices. Il s’agit plus souvent d’arthralgies inflammatoires que d’oligoarthrite ou de vraie polyarthrite. Elle concerne essentiellement les petites et les grosses articulations sur un mode asymétrique, intermittent et parfois migrateur. Par définition, elle est séronégative, non érosive ni déformante (sauf association à une vraie polyarthrite rhumatoïde sous-jacente).
En parallèle, une atteinte axiale spécifique (en particulier du rachis cervical ou lombaire) est possible au cours de la PCA, et doit faire évoquer une véritable spondyloarthrite associée surtout en cas de lésions radiologiques compatibles. D’autres manifestations rhumatologiques telles que les tndinites, ténosynovites, ou autres atteintes péri-articulaires sont possibles.
Manifestations oculaires
L’atteinte oculaire est fréquente (environ 1 patient sur 2), pouvant précéder l’apparition des chondrites de plusieurs années [9]. Les manifestations les plus fréquentes sont l’épisclériteet la sclérite. Cette dernière est probablement l’atteinte oculaire la plus grave, pouvant évoluer vers une scléromalacie résiduelle, à l’origine d’une perforation du globe oculaire, et semble associée aux chondrites nasales et auriculaires. Les autres atteintes rencontrées sont par ordre de fréquence la kérato-conjonctivite sèche simple ou ulcérée (parfois en rapport avec un syndrome de Gougerot-Sjögren associé), l’uvéite, l’atteinte rétinienne et l’atteinte du nerf optique pouvant évoluer vers une véritable atrophie du nerf optique. Devant une uvéite non granulomateuse on doit se poser la question du diagnostic différentiel de spondyloarthrite voire d’une spondyloarthrite associée.
Manifestations cardio-vasculaires
L’atteinte cardiaque est observée chez environ 15% des malades, survenant de façon tardive au cours de la maladie, et représente l’une des principales causes de mortalité.
Il s’agit le plus souvent d’une valvulopathie (≈10% des patients au cours de l’évolution) de type insuffisance aortique par dilatation de l’anneau le plus souvent, plus rarement d’insuffisance mitrale. L’insuffisance aortique est d’évolution progressive, et doit faire dépister un anévrysme de l’aorte thoracique ascendante associé. L’extension anévrysmale aux gros troncs artériels et à l’aorte abdominale est plus rare.
L’innervation intrinsèque du cœur peut également être lésée, responsable de troubles de la conduction ou du rythme qui peuvent être plus ou moins réversibles après traitement.
Une péricardite ou une vascularite des moyens (dont artères coronaires) et des petits vaisseaux ont été décrites. Selon Michet, 5 à 14 % des patients présenteraient une vascularite leucocytoclasique cutanée et 10 % une atteinte microvasculaire systémique responsable de complications neurologiques périphériques et centrales. Plus rarement, il peut exister une artérite des gros vaisseaux voisine de l’artérite de Takayasu ou de l’artérite à cellules géantes. L’histologie montre alors un infiltrat lymphocytaire de la paroi des vasa vasorum avec fragmentation et destruction du tissu élastique de la limitante élastique externe, évoluant vers une hyalinisation de la paroi aortique.
Atteinte cutanée
L’atteinte cutanée est multiple et non spécifique, survenant chez 25 à 30% des patients au cours de l’évolution de la maladie.
Ont été décrits : aphtose buccale, nodules des membres supérieurs ou inférieurs, purpura, papules, pustules aseptiques, phlébites superficielles, livédo réticularis, ulcérations des membres, nécroses des extrémités, dermatoses neutrophiliques dont le syndrome de Sweet ou des lésions d’erythema elevatum diutinum, urticaire et angioedème.
En cas d’aphtose importante, il est important de rechercher d’autres signes pouvant évoquer l’existence d’un MAGIC syndrome (pour « Mouth And Genital ulcers with Inflamed Cartilages »), décrit par certains auteurs comme une forme de chevauchement entre maladie de Behçet et PCA.
Plus de 90% des patients présentant une PCA associée à une myélodysplasie présentent des signes cutanés si bien que, chez le sujet âgé, l’atteinte cutanée de la PCA doit faire systématiquement rechercher une myélodysplasie sous-jacente.
Autres atteintes
Les formes neurologiques sont rares et concernent essentiellement le système nerveux central sous forme d’atteinte des nerfs crâniens. D’autres atteintes ont été décrites et sont proches de celles rencontrées dans les vascularites cérébrales (déficit focal, épilepsie, méningite, rhombencéphalite…). Cependant, une neuropathie périphérique peut se voir en cas de vascularite associée.
L’atteinte rénale spécifique de la PCA reste véritablement exceptionnelle (<2% des patients au cours de l’évolution de la maladie) et doit avant tout conduire à remettre en question le diagnostic de PCA. Les principaux diagnostics différentiels sont la granulomatose avec polyangéite (GPA, ex-Wegener) et la polyangéite microscopique (MPA).

DIAGNOSTIC de la polychondrite
Il n’existe aucune anomalie biologique spécifique de PCA permettant de porter le diagnostic de façon certaine :
– Syndrome inflammatoire biologique habituel, avec environ 10% des patients gardant une CRP normale pendant les poussées inflammatoires.
– Les anticorps anti-collagène de type II, anti-matrilline-1 et anti-labyrinthine ne doivent pas être recherchés en pratique courante en raison de leur faible sensibilité et spécificité, tout comme le typage HLA.
– Des anticorps anti-nucléaires sont détectés, après exclusion des cas associés à un lupus ou une connectivite mixte, chez environ 10% des patients
– Des anticorps dirigés contre le cytoplasme des polynucléaires neutrophiles (ANCA) peuvent être retrouvés. Leur mise en évidence doit faire évoquer le diagnostic différentiel de granulomatose avec polyangéite (ex-Wegener), surtout s’il existe une spécificité anti-PR3.
– Un syndrome myélodysplasique est systématiquement recherché chez les sujets âgés, notamment chez le sujet de plus de 60 ans et de sexe masculin. Il est dépisté par une simple numération formule-sanguine plaquette et frottis sanguin. La moindre anomalie dans ce contexte doit motiver facilement la réalisation d’un médullogramme avec caryotype, dans la mesure où le pronostic vital dépend en général de l’hémopathie et non de la PCA.
Le diagnostic de PCA est pratiquement impossible à établir avec certitude avant l’apparition des chondrites, qui peuvent parfois survenir plusieurs années plus tard. Aucun examen de laboratoire ou d’auto-anticorps ne permet de porter avec certitude le diagnostic de PCA, qui repose généralement sur un faisceau d’argument, dont la présence de chondrites et l’élimination des quelques diagnostics différentiels (par exemple granulomatose avec polyangéite, GPA).
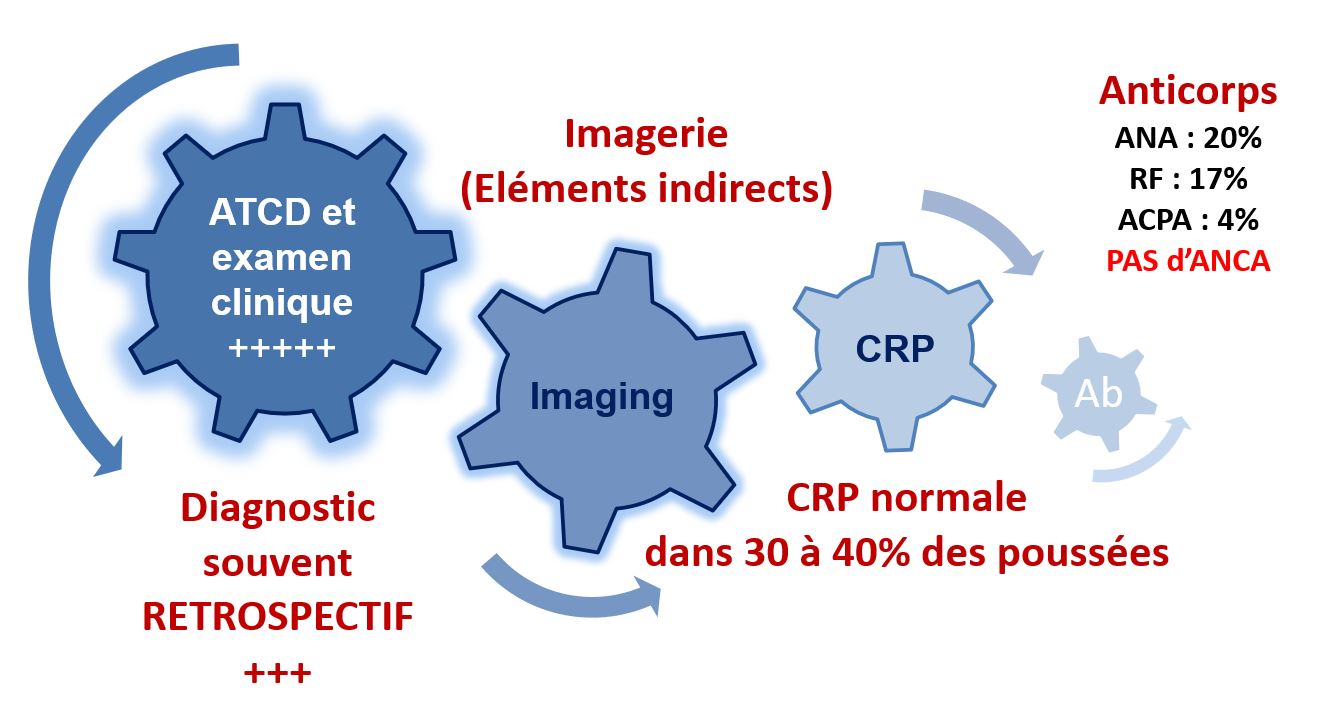
Le bilan diagnostic initial comporte généralement un bilan biologique visant à rechercher un syndrome inflammatoire (qui peut être absent dans 40% des poussées), éliminer les principaux diagnostics différentiels (par exemple une vascularite à ANCA), recherche une éventuelle autre maladie auto-immune associée (présente dans 20 à 30% des cas), recherche des signes indirects d’atteinte des cartilages ou d’atteinte d’organes par un bilan radiologique adapté, et rechercher d’éventuelles contre-indications aux traitements. Ce bilan diagnostic initial comporte habituellement un bilan biologique standard, une recherche de syndrome inflammatoire (CRP), un bilan immunologique (anticorps anti-nucléaires et anti-ENA, facteur Rhumatoïde et anti-CCP, ANCA), une TDM des sinus et du thorax visant à éliminer certains diagnostics différentiels tels que la GPA, et tout autre examen approprié en fonction du contexte clinique et des éventuelles atteintes d’organe suspectées (par exemple EFR, échocardiographie, imagerie de l’aorte, etc). La biopsie de cartilage n’est pas recommandée, car elle ne montre habituellement qu’un infiltrat inflammatoire non spécifique, mais une biopsie de la muqueuse nasale peut être discutée en cas de doute avec une forme localisée de GPA.
causes de la polychondrite
La pathogénie de la PCA est encore mal élucidée. La destruction du cartilage est liée à son infiltration par des cellules inflammatoires. Des auto-anticorps dirigés contre le collagène (principalement de type II, mais aussi IX, X et XI) et la matrilline-1 ont été mis en évidence chez les patients atteints de PCA, tout comme des anticorps anti-labyrinthine. Cependant, ces anticorps sont trop peu sensibles pour pouvoir être utilisés en pratique clinique. Des lymphocytes T auto-réactifs dirigés contre certains collagènes ont par ailleurs pu être détectés. Les concentrations sériques de certaines cytokines sont augmentées pendant la phase active de la maladie, dont la monocyte chemo-attractant protein 1 (MCP-1), le macrophage inflammatory protein 1 beta (MIP-1beta) et l’Interleukine-8 (IL-8), ce qui souligne le rôle des macrophages au cours de cette pathologie. L’injection à des rats de matrilline-1, une protéine spécifique du cartilage trachéal, reproduit l’atteinte respiratoire de la PCA [8]. Enfin, la PCA est associée génétiquement aux allèles HLA-DRB1*0, DRB1*13, DRB1*14 et HLA-DQA1et B1 mais le typage HLA n’a pas non plus d’intérêt pratique.
TRAITEMENT de la polychondrite
La PCA est une maladie capricieuse, évoluant sous la forme de poussées entrecoupées de périodes de rémission qui peuvent être très prolongées. Une majorité des patients présentera des rechute, justifiant l’utilisation du terme « chronique » dans le nom de la maladie. Les principaux objectifs de la prise en prise en charge de la PCA sont le contrôle de l’activité et des poussées inflammatoires de la maladie, la prévention des rechutes et des séquelles, le maintien d’une qualité de vie la plus optimale possible, et dans certains cas la prise en charge des complications telles que la myélodysplasie, qui peut entrainer une dépendance transfusionnelle, ou des séquelles.
La prise en charge thérapeutique de la PCA est complexe, et dépend de la nature des manifestations présentées par le patient. Certaines formes mineures pourront être traitées par des AINS mais dans la majorité des cas, la stratégie thérapeutique repose sur l’utilisation d’un traitement permettant de contrôler la poussée inflammatoire (par exemple corticothérapie) et un traitement de fond, tel que la colchicine, la dapsone, les immunosuppresseurs conventionnels (par exemple le méthotrexate) ou les traitements biologiques, sachant qu’il n’existe aucun essai randomisé permettant d’identifier la stratégie de prise en charge optimale, qui repose sur un consensus d’experts.
Les anti-inflammatoires non stéroïdiens (AINS) peuvent être utilisés dans les formes limitées de PCA comme par exemple les sclérites et les épisclérites, et peuvent alors même être utilisés sous forme de collyre. Ils peuvent s’avérer également efficaces dans les formes peu sévères de chondrites auriculaires et nasales, et d’arthrites.
La Colchicine peut être efficace dans les formes articulaires périphériques peu sévères.
Enfin, on peut proposer de la Dapsone en traitement de fond des formes non sévères de chondrite auriculaire et nasale et d’arthrite. Son efficacité semble cependant limitée.
Les immunosupresseurs
Souvent très efficaces, on les utilise dans la très grande majorité des cas afin de traiter les atteintes résistantes aux AINS, ou d’emblée dans les formes sévères (atteinte ophtalmologique sévère, atteinte laryngée, trachéale ou bronchique, atteinte cardiaque, atteinte de l’oreille interne d’installation récente et vascularite systémique). Selon le type d’atteinte à prendre en charge, la posologie adéquate en équivalent Prednisone varie entre 0,25 et 1 mg/kg/jour. On initie parfois ce traitement, si l’on souhaite une efficacité rapide, par des bolus IV de 500-1000 mg de Méthylprednisolone sur 3 jours. Il n’existe pas de règle concernant la durée du traitement d’attaque et sa décroissance. Parfois, un sevrage complet et définitif est possible, mais il est plutôt d’usage, afin d’éviter les rechutes, de maintenir une dose faible (5-10mg/j) au long cours
Les immunosuppresseurs Le choix de la molécule est encore empirique. On utilise les immunosuppresseurs chez les patients cortico-intolérants ou corticodépendants, ou encore d’emblée dans les formes viscérales graves. On utilise classiquement le Méthotrexate, l’Azathioprine, le Cyclophosphamide et la Ciclosporine. De façon plus récente, le Mycophenolate mofetil est lui aussi utilisé, tout comme l’Azacitidine dans les formes associées à un syndrome myélodysplasique, qui a été utilisé avec succès chez 4 patients d’une série récente
Les biothérapies C’est surtout l’avènement des biothérapies qui a récemment amélioré le spectre des possibilités de traitement des PCA graves ou cortico-résistantes. L’infliximab a longtemps été utilisé en raison d’une efficacité chez environ la moitié des patients, mais avec de fréquentes pertes d’efficacité et des effets secondaires infectieux. L’etanercept semble également efficace.
Plus récemment, l’efficacité du Tocilizumab (anti-Interleukine 6) a été rapportée chez quelques patients avec des atteintes sévères et réfractaires à de nombreuses lignes thérapeutiques. L’anakinra (IL-1RA) semble être efficace, avec quelques cas publiés. Ce traitement semble intéressant dans la mesure où le risque infectieux est moindre par rapport aux anti-TNF alpha. L’abatacept (analogue du CTLA-4) a également montré son efficacité en cas de résistance à 3 anti-TNF et à un anti-IL1.
L’utilisation du Rituximab semble quant à elle décevante, seule une étude sur 9 patients, a montré une amélioration partielle chez deux patients sous ce traitement
Autres traitements systémiques
N’ayant pas ou peu d’effet immunosuppresseur, le Leflunomide ou encore les Immunoglobulines forte dose par voie intraveineuse peuvent avoir une certaine efficacité dans la PCA.
Traitements locaux Les atteintes laryngée, trachéale et bronchique peuvent parfois nécessiter des gestes locaux tels que des infiltrations par glucocorticoïdes, la pose d’une endoprothèse ou d’une trachéostomie, une dilatation mécanique, une résection chirurgicale voire si possible une reconstruction trachéale. Les atteintes valvulaires et aortiques sont par ailleurs traitées chirurgicalement, d’où l’importance d’une surveillance régulière.
POLYCHONDRITE ATROPHIANTE
LA RECHERCHE SUR LA POLYCHONDRITE AU CENTRE DE REFERENCE DE STRASBOURG
Le centre de référence de Strasbourg est particulièrement impliqué dans la recherche autour de la polychondrite atrophiante :
1) Le centre de référence de Strasbourg a un rôle moteur dans la recherche au cours de la polychondrite, et coordonne (Senior coordination) la recherche sur la polychondrite en Europe au sein de l’union Européenne (ERN-ReCONNET).
2) Le centre de référence de Strasbourg a développé les 2 scores principaux permettant d’évaluer les patients atteints de polychondrite : score d’activité RPDAI et score de séquelle RPDAM (Professeur Laurent Arnaud), et a développé une collaboration avec le National Institute of Health (NIH) des Etats-Unis pour ces scores.
3) Le centre de référence de Strasbourg rend des avis (télémédecine) concernant la prise en charge des patients atteints de polychondrite dans le cadre de son activité de centre de référence.
